Se ti stai chiedendo cosa sono gli isomeri devi sapere che, derivando dal greco “isos” (uguale) e “meros” (parte), essi racchiudono quei composti con stessa formula bruta e identica massa molecolare, ma con differenti proprietà chimiche e fisiche ⚛️
La diversità degli isomeri è dovuta al diverso modo in cui gli atomi si legano e si organizzano tra loro.
In sostanza, questi composti sono come cugini nella grande famiglia delle molecole: condividono alcuni tratti, ma ognuno ha la sua unicità 🔎
Gli isomeri sono un concetto che sembra complesso, ma con il giusto approccio può diventare molto interessante e affascinante.
I corsi ADT ti offrono:
- simulazioni illimitate con oltre 36.000 quiz ministeriali e tantissime modalità di esercitazione sulla nostra piattaforma Futura 💯
- chat diretta con il tuo tutor personale per ottenere supporto anche dopo l’orario di lezione 📚
- materiale di studio completo 📖
- lezioni in diretta e on demand con docenti qualificati ed esperti nella preparazione ai test 🧠
Nei prossimi scroll (come avrai intuito) ci concentreremo sugli isomeri, un argomento fondamentale in chimica e spesso presente nei test d’ingresso. Scopriamo insieme cosa sono e perché sono così importanti.
Isomeri: definizione e classificazione
La scienza che studia gli isomeri viene definita isomeria e si incentra sulle differenze che caratterizzano i composti con medesima formula bruta.
Infatti, identificare un isomero richiede attenzione alla formula molecolare e alla struttura. La chiave sta nel notare se due composti con la stessa formula bruta hanno strutture diverse (isomeri di struttura) o un diverso orientamento degli atomi nello spazio (stereoisomeri) 🤔
Proprio per questo in chimica si possono trovare diversi isomeri, che vengono suddivisi in due macro-categorie principali:
- isomeri di struttura
- stereoisomeri
Ora è necessario addentrarci nell’analisi di questi composti chimici e analizzare le tipologie esistenti cercando si capirne le differenze 🔎
Isomeri di struttura
Gli isomeri di struttura presentano sempre la stessa formula bruta, ma i legami sono differenti e di conseguenza possono presentare caratteristiche fisiche e chimiche completamente diversi.
L’isomero strutturale più “famoso” è il butano con formula bruta C4H10, quattro legami di carbonio e uno di idrogeno. Cambiando i legami otteniamo due isomeri strutturali:
- n-butano
- isobutano
Attraverso la rappresentazione grafica degli isomeri del butano comprendiamo che non cambia la massa molecolare. I legami diversi invece creano l’isobutano, che è un fluido refrigerante che non ha niente a che vedere con il gas 🧪
Gli isomeri di struttura (chiamati anche costituzionali) presentano ulteriori suddivisioni e sottocategorie 🤔
Isomeri di Catena
Questi isomeri differiscono nella disposizione dello scheletro di carbonio. Alcuni sono lineari, altri ramificati, ma con proprietà fisiche differenti.
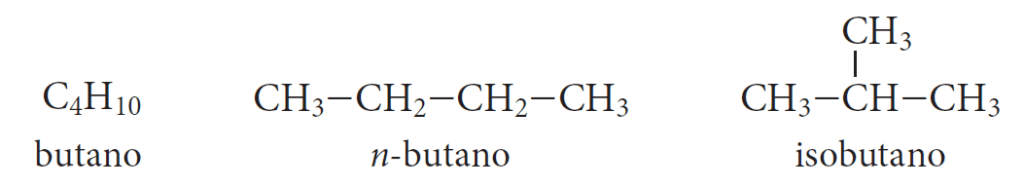
Prendendo come esempio il pentano, con formula bruta C5H12, si possono formare tre diversi isomeri:
- n- pentano: (CH3)2CHCH2CH3
- isopentano: (CH3)2CHCH2CH3
- neopentano: C(CH3)4
Come possiamo vedere, in questo caso cambiano solo le catene di carbonio e tutto il resto rimane invariato. Per comprendere meglio la differenza vediamo quali sono le caratteristiche fisiche e chimiche diverse dei tre isomeri del pentano:
- n-pentano e isopentano sono due liquidi altamente infiammabili, incolore e dall’odore simile alla benzina ⛽️
- neopentano è un gas volatile e infiammabile 🔥
Quindi il legame diverso degli atomi di carbonio con la catena carboniosa cambia le caratteristiche chimiche e fisiche di ogni isomero.
Isomeri di Posizione
Gli isomeri di posizione sono una classificazione interessante in cui i composti differiscono per la posizione del gruppo funzionale lungo la catena carboniosa.
Il caso più emblematico di isomero di posizione è un alchene derivante dal butano, l’1-butene con formula bruta C4H8.
In questo composto la posizione del doppio legame cambia e si creano due isomeri di posizione:
- 1- butene 🧪
- 2- butene ⚗️
La struttura dell’1-butene è CH2 = CH-CH2-CH3, mentre quella del 2-butene è CH3-CH= CH- CH3 ⚛️
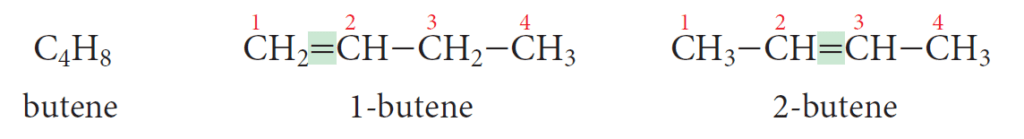
L’unica differenza tra le due riguarda la posizione del doppio legame, che è in grado di modificare le proprietà fisiche e chimiche.
Per esempio, i reagenti possono attaccare il doppio legame in modi diversi a seconda della sua posizione, portando a prodotti diversi. Questo aspetto è cruciale nella chimica organica, specialmente nella sintesi e nella reattività dei composti 🧑🔬
Isomeri di Gruppo Funzionale
In questa classificazione troviamo gli isomeri con la stessa formula bruta, ma con gruppi funzionali organizzati in modi diversi.
In chimica, vi sono tantissimi gruppi funzionali che hanno la capacità di determinare le caratteristiche fisiche e chimiche dei composti (alcoli, fenoli, chetoni, ecc.)
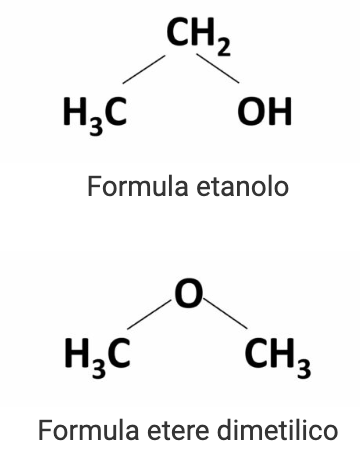
Se prendiamo la formula bruta C2H6O, ci troveremo con due composti differenti. Con una diversa disposizione degli atomi si creano differenti gruppi funzionali:
- l’etanolo C2H5OH (alcol etilico) 🍺
- l’etere dimetilico CH3OCH3 💊
La differenza è lampante perché l’alcool etilico è un liquido e viene usato in tutte le bevande alcoliche, invece l’etere dimetilico è un gas incolore utilizzato in ambito chimico e industriale.
Stereoisomeri
Questa macro-categoria è caratterizzata da isomeri sia con la medesima formula bruta, sia con gli stessi legami. In tal caso, gli atomi si dispongono nello spazio in maniera diversa e quindi nella rappresentazione grafica sono riconoscibili come composti differenti.
Gli isomeri hanno tante sottili differenze tra loro e anche gli stereoisomeri presentano altre suddivisioni.
Isomeri configurazionali
Questi isomeri, divisi ulteriormente in isomeri ottici e geometrici (cis-trans), condividono la stessa formula strutturale, ma differiscono nell’orientamento spaziale degli atomi ⚛️
Gli isomeri ottici hanno la stessa formula strutturale, ma presentano un’immagine speculare che non può essere sovrapposta. Ciò vuol dire che questi composti, sebbene abbiano le stesse proprietà fisiche e chimiche, si comportano in modo diverso quando interagiscono con la luce polarizzata 🤔
La classificazione geometrica (cis-trans), invece, è caratterizzata da composti che si formano quando cambia la posizione degli atomi nello spazio rispetto a un doppio legame o a un anello.
Nei composti con legame doppio o ad anello, come gli alcheni o i cicloalcani, i gruppi attaccati agli atomi di carbonio coinvolti nel doppio legame possono essere orientati in due modi diversi:
- il composto è detto “cis” quando i gruppi simili o gli stessi atomi sono sullo stesso lato del doppio legame. Per esempio, se nel 2-butene i due gruppi metile sono sullo stesso lato del doppio legame ci troviamo di fronte alla forma “cis” del 2-butene.
- il composto è detto “trans” quando i gruppi o gli atomi si trovano su lati opposti del doppio legame. Utilizzando lo stesso esempio del 2-butene, la forma è “trans” se un gruppo metile si trova su un lato del doppio legame e l’altro sul lato opposto.
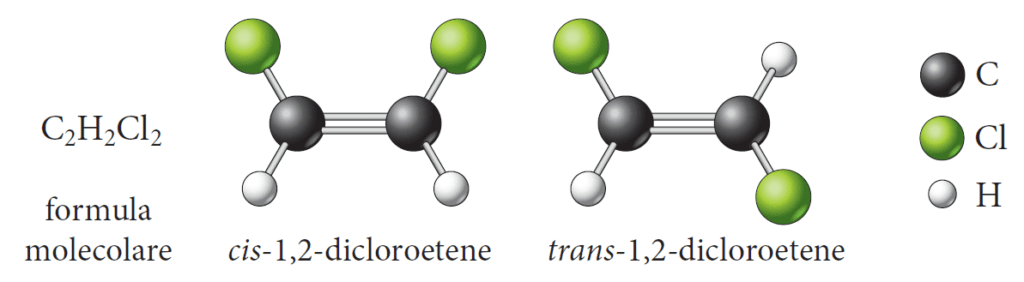
La differenza nella disposizione spaziale porta a proprietà fisiche e chimiche diverse tra gli isomeri -cis e -trans, implicando usi diversi in chimica organica, farmaceutica e biologia 🧪
Isomeri conformazionali
In questa classificazione rientrano gli isomeri formati dalla rotazione attorno ai legami semplici C-C, creando diverse disposizioni spaziali 📐
Tale tipo di isomeria si manifesta in due forme: eclissata e sfalsata. Per esempio, nel butano, la rotazione attorno al legame centrale C-C può produrre diverse disposizioni degli atomi di idrogeno e di carbonio, con effetti significativi sulle proprietà fisiche e chimiche del composto.
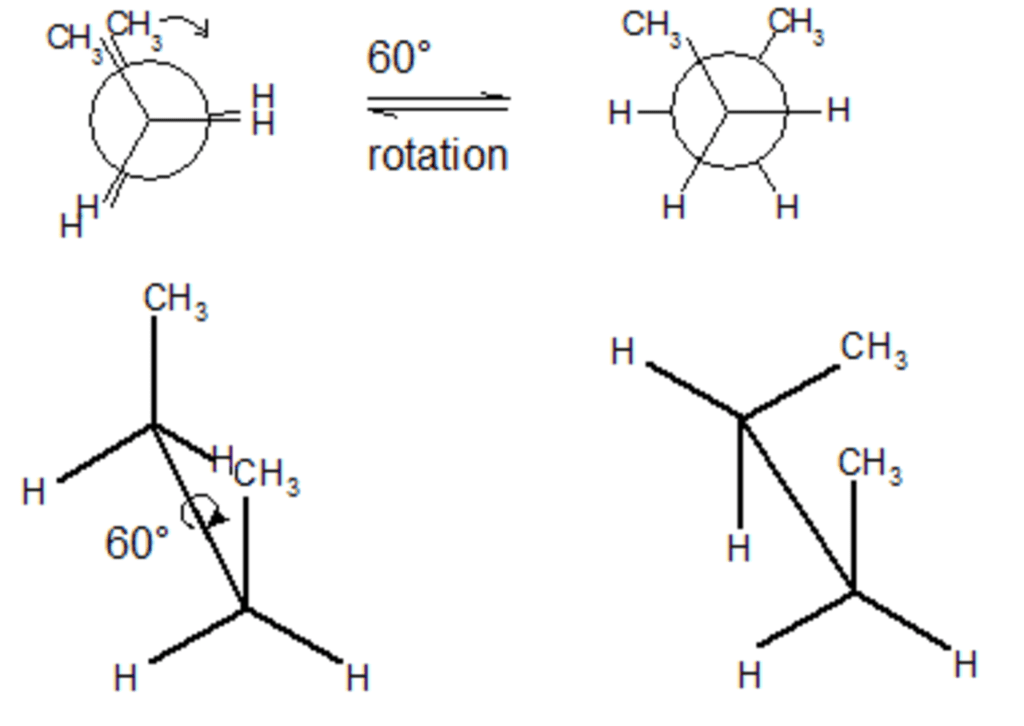
Gli isomeri conformazionali possono inter-convertirsi semplicemente con il movimento dei legami chimici, senza romperne o formarne di nuovi. Tale capacità conferisce a queste molecole una flessibilità unica, che è essenziale in molti processi biologici e chimici ⚛️
L’importanza degli isomeri in chimica e biologia
Gli isomeri ci fanno capire come piccole variazioni portano a differenze sostanziali.
Rianalizziamo il butano (C4H10): se cambiamo i legami otteniamo n-butano e isobutano, che hanno la stessa formula bruta, ma strutturalmente e funzionalmente sono diversi ⛽️
Lo stesso vale per l’etanolo (C2H5OH) e l’etere dimetilico (CH3OCH3), che pur condividendo la formula C2H6O sono sostanze completamente diverse.
Un altro esempio di isomeria è rappresentato da glucosio e fruttosio. Entrambi hanno la formula C6H12O6, ma la loro diversa struttura influisce notevolmente sul modo in cui vengono metabolizzati nel corpo umano.
Mentre il glucosio è essenziale per molte funzioni corporee, un’eccessiva assunzione di fruttosio può portare a complicazioni sanitarie 🩺
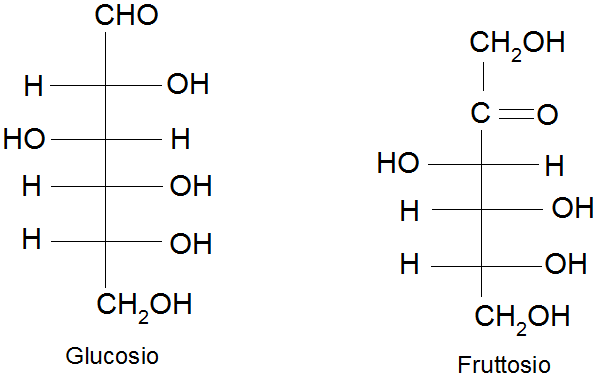
Come puoi vedere capire cosa sono gli isomeri e come sono classificati ti aiuta a capire meglio la chimica organica e a risolvere gli esercizi senza difficoltà 🧠
Per ripassare in modo approfondito gli isomeri e tutti gli argomenti di chimica organica per il test facendo un po’ di pratica con gli esercizi, c’è Futura 💯
In più, se durante lo studio ti sorgono dubbi o domande, non esitare a chiedere spiegazioni o consigli. Unisciti alla nostra community Telegram con più di 6000 studenti per confrontati su esercizi e argomenti del test di ammissione 💬







